Het Anabolenboek
Willem Koert
Aede de Groot
Wageningen, 1/9/2007
17. Ethers en Stikstofderivaten
Aede de Groot, Willem Koert
Verreweg de meeste hormoonderivaten zijn esters. De industrie heeft echter ook THP-ethers, acetalen, enol-ethers, gewone ethers, silyl-ethers en stikstofderivaten van steroiden ontwikkeld en op de markt gebracht. Die komen in dit hoofdstuk aan de orde.
Mensen hebben geen enzymen in hun bloed of in hun spieren die THP-ethers, acetalen, enol-ethers, gewone ethers, silyl-ethers of stikstofderivaten van steroiden kunnen hydrolyseren, zoals dat wel gebeurt met esters. De meeste van deze derivaten hydrolyseren wel onder invloed van maagzuur. Slik je ze, dan gaan de verbindingen in de maag al kapot. Daar komt het werkzame steroid dan al vrij. Als we deze derivaten injecteren, dan komen de actieve steroiden meestal pas vrij in de lever, waarschijnlijk na een oxidatie door een cytochroom P450-enzym.
Tetrahydropyranyl-ethers (THP-ethers) en andere acetalen
Chemici gebruiken THP-ethers om hydroxylgroepen tijdelijk te beschermen tegen ongewenste reacties. Later kunnen ze de THP-groep gemakkelijk verwijderen door hydrolyse met verdund zuur. Dan verdwijnt de THP-groep en hydroxylgroep keert terug. Achter de anabole steroiden die op de markt zijn gebracht als THP-ether zat hetzelfde idee. Het lichaam kan de THP-groep verwijderen en zo het vrije werkzame steroid vormen.
THP-ethers van steroiden zijn maar voor een deel ethers, ook al staat het woord ether in de naam. Een ether kun je in twee stappen afleiden van water door de H-atomen te vervangen door alkylgroepen. In Schema 1 is eerst één H-atoom in water vervangen door een alkylgroep. Dan krijgen we alcohol. In dit voorbeeld ethanol, de gewone alcohol in bier, wijn en sterkere dranken. Als we ook het tweede H-atoom vervangen door een alkylgroep, krijgen we een ether. In Schema 1 is dit opnieuw gedaan met een ethylgroep. Dan ontstaat diethylether of gewone ether. In een ether hebben beide C-atomen naast het O-atoom maar één binding naar dat O-atoom.
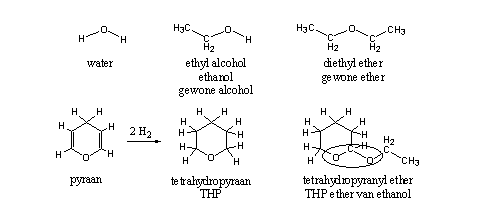
Schema 1
Een zesring met een O-atoom en twee dubbele bindingen in de ring heet een pyraan. Als we de beide dubbele bindingen elk met twee H-atomen reduceren, komen er vier H-atomen in het molecuul en krijgen we tetrahydropyraan (zie Schema 1). Als dat structuurelement de plaats inneemt van het tweede H-atoom aan het O-atoom in ethanol, dan krijgen we de tetrahydropyranyl-ether van ethanol. Tot zover is alles hetzelfde in de bovenste en de onderste rij van Schema 1. Toch zijn er verschillen tussen de beide ethers.
Aan de rechterkant van het O-atoom is alles gelijk, maar aan de linkerkant niet. In diethylether heeft het linker C-atoom bovendien maar één binding naar het O-atoom, in de tetrahydropyranyl-ether heeft dat C-atoom twee bindingen naar twee O-atomen.
Dit ogenschijnlijk kleine verschil in structuur betekent dat die groep andere chemische eigenschappen heeft dan een gewone ether, en ook een andere naam heeft. Deze groep is omcirkeld in de structuurformule en heet acetaal. Acetalen hydrolyseren gemakkelijk onder zure omstandigheden, ethers doen dat niet (zie Schema 2). De verklaring voor dit verschil in reactiviteit is bekend maar het gaat te ver daar hier op in te gaan.
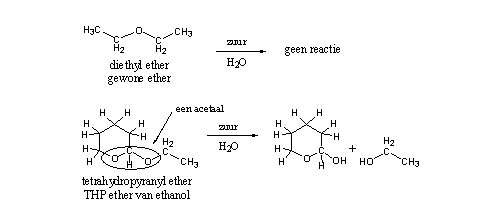
Schema 2
In de maag zit maagzuur. Chemici kennen dat beter als zoutzuur (HCl) en dat is een sterk zuur. Maagzuur zorgt in de maag voor een zuurgraad tussen de 1 en 2, en dat is behoorlijk zuur. Chemici geven de zuurgraad aan met een pH-waarde. Gewoon water heeft een pH van 7, en dat noemen we neutraal. Een pH tussen 0 en 7 noemen we zuur en een pH tussen 7 en 14 heet basisch. In de darm is de omgeving een beetje basisch met een pH van 7-8, in het bloed en in de spieren ligt de pH rond de 7.
Acetalen, zoals THP ethers, hydrolyseren gemakkelijk onder zure omstandigheden. Dat betekent dat THP-ethers van steroiden die we oraal innemen, al in de maag hydrolyseren tot het werkzame anabool. Dat is niet zo gunstig, want het vrije steroid moet dan nog steeds de darm en de lever passeren, voordat het in het bloed komt en de spieren kan bereiken. Er is daardoor tijd en gelegenheid voor metabole omzettingen tot inactieve metabolieten.
We kunnen een THP-ether ook injecteren, maar de steroid-THP-ether zelf is niet actief. Als het derivaat de maag niet passeert, moet de THP-ether er op een andere manier afgehaald worden. In het bloed en in de spieren ligt de pH rond de 7 en onder die omstandigheden gaan THP-ethers er niet af. Zoals gezegd hebben we ook geen enzymen in het bloed die THP-ethers kunnen hydrolyseren, zoals we wel enzymen hebben die esters hydrolyseren.
In de lever zitten echter wel cytochroom P450-enzymen die THP-ethers kunnen oxideren. Een mogelijke gang van zaken is weergegeven in Schema 3. De oxidatie vindt waarschijnlijk plaats naast het O-atoom in de tetrahydropyraanring. Het gevormde oxidatieproduct valt daarna spontaan uiteen in een dialdehyde en het vrije steroid. Het schema is een beetje speculatief, want er is weinig onderzoek gedaan naar het metabolisme van THP-ethers.
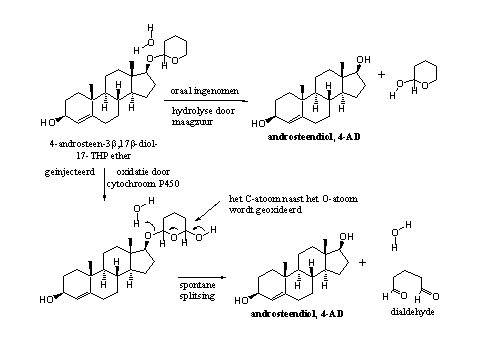
Schema 3
De lever zal het vrije steroid verder omzetten in glucuroniden en/of sulfaat-esters. Het vrije steroid kan ook aan het Sex Hormone Binding Globuline (SHBG) binden, en op die manier geinactiveerd worden. Waarschijnlijk zal maar weinig van het vrije steroid de spiercel bereiken.
Er is dus een duidelijk verschil tussen esters en THP-ethers van anabole steroiden. Esters moet je injecteren en enzymen in het bloed maken dan het werkende anabool vrij. Oraal ingenomen THP-ethers hydrolyseren onder invloed van maagzuur. Geinjecteerde THP-ethers worden in de lever geactiveerd.
Het maakt dan ook weinig uit of je het anabool zelf slikt of de THP-ether daarvan. Dat er zoveel anabole steroiden als THP-ether in designer-supplementen verschijnen heeft waarschijnlijk meer te maken met het omzeilen van wettelijke regels of lopende patenten, dan met het streven naar betere producten door fabrikanten. In Figuur 1 hebben we een aantal THP-ethers van anabole steroiden weergegeven die we in designer-supplementen hebben aangetroffen.
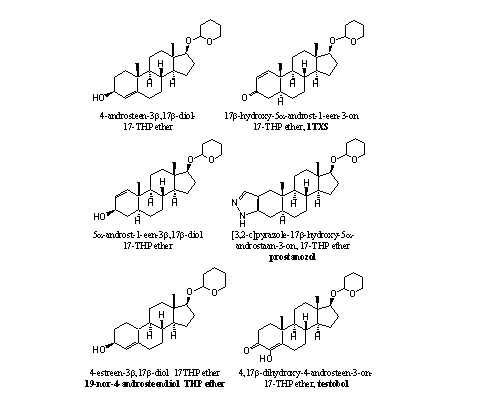
Figuur 1
Acetalen van steroiden kunnen ook in andere vormen verschijnen dan in die van een THP-ether. Een voorbeeld is het dubbel-acetaal van testosteron (zie Figuur 2) [1]. Het C3-atoom in ring A heeft twee bindingen naar twee O-atomen en is dus een acetaal. De betreffende groep heet een dioxolan-groep. Chemici gebruiken deze groep vaak om een carbonylgroep tijdelijk te beschermen.
Het middelste C-atoom in de zijstaart aan de C17-hydroxylgroep heeft ook twee bindingen naar twee O-atomen. Deze methoxymethylgroep is daarom ook een acetaal. Onder invloed van verdund zuur (maagzuur) zullen beide acetalen hydrolyseren. Bij orale toediening is de activiteit van dit derivaat inderdaad vergelijkbaar met die van testosteron.
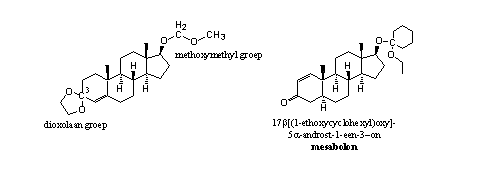
Figuur 2
In mesabolon (zie Figuur 2) zit het acetaal aan de 17b-hydroxylgroep. Omdat aan het C-atoom in de cyclohexylring een tweede O-atoom zit, is dit derivaat een acetaal. We mogen aannemen dat bij orale inname ook dit derivaat al in de maag zal hydrolyseren.
Er zijn tientallen van die beschermende acetalen bekend, maar de THP-ether en de dioxolan-groep zijn het meest bekend [2]. Mogelijke andere acetalen voor de C17-hydroxylgroep staan in Figuur 3.
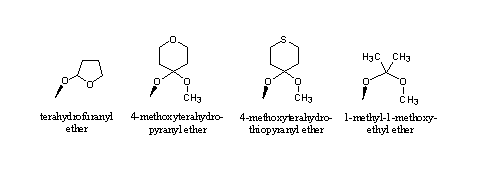
Figuur 3
Het vijfring-acetaal, de tetrahydrofuranyl-(THF)-ether, hydrolyseert wat sneller dan het al bekende zesring-acetaal, de tetrahydropyranyl-(THP)-ether. Dit komt omdat in de tetrahydrofuranyl-ether de spanning in de ring groter is, en de sterische hinder dus kleiner is.
Ook in de andere structuren is het acetaal te herkennen, ze lijken op het acetaal rechts in Figuur 2. Elke structuur is net iets anders. Daardoor hebben ze ook allemaal een net iets andere hydrolyse-snelheid. Bij oraal ingenomen derivaten zullen deze groepen er zonder uitzondering in de maag (bj pH 2) al af gaan. Het heeft weinig zin deze groepen aan een anabool steroid te hangen. Het gedrag bij injectie kunnen we alleen te weten komen door de derivaten te testen.
Enol-ethers
Een enol is een hydroxylgroep die direct aan één van de C-atomen van een dubbele binding zit. Als we in het enol, net als in ethanol, het tweede H-atoom aan het O-atoom vervangen door een alkylgroep, dan krijgen we een enol-ether (zie Schema 4).
Enol-ethers lijken in hun chemisch gedrag op acetalen. Enol-ethers hydrolyseren ook onder zure omstandigheden tot een carbonylverbinding en een hydroxylverbinding. De details van deze hydrolyse zijn bekend, maar we geven hier alleen het eindresultaat. We kunnen beide uitkomsten van de hydrolyse, hydroxylgroep en/of carbonylgroep, gebruiken voor het vrijmaken van het steroid uit het enol-ether-derivaat (zie Schema 4).
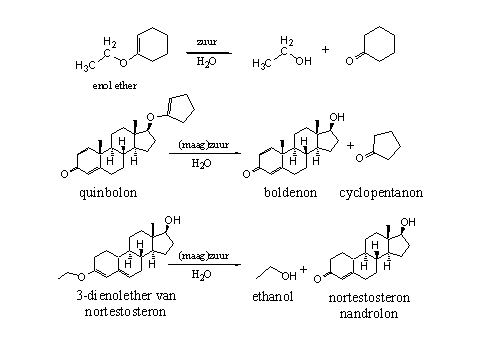
Schema 4
In het voorbeeld van de enol-ether quinbolon komt bij hydrolyse in de zure omgeving van de maag, de hydroxylgroep aan C17 vrij, onder vorming van boldenon en cyclopentanon. In het tweede voorbeeld in Schema 4 gaat het om een dienol-ether, waarbij de 4-een-3-on groep van nandrolon vrijkomt na hydrolyse [3].
Wat we eerder opmerkten over THP-ethers geldt ook voor enol-ethers. Als je ze slikt, dan hydrolyseren enol-ethers al in de maag onder invloed van maagzuur. Het slikken van zo’n derivaat werkt dan ook net zo goed of net zo slecht als het slikken van het anabole steroid zelf. Er zijn ook in dit geval geen enzymen bekend die geinjecteerde (di)enol-ethers van steroiden kunnen hydrolyseren. In de lever kan weer wel oxidatie optreden waardoor het werkzame steroid vrijkomt.
In voedingssupplementen hebben we nog een mooie combinatie van een THP ether met een dienol-ether gevonden (zie Schema 5). Het is een derivaat van de aromataseremmer 6-OXO. Ook hier is het tamelijk zinloos dit derivaat te slikken in plaats van 6-OXO zelf. Na de splitsing van de dienol-ether of van de THP-ether krijgen we de bekende 4-een-3-on structuur terug.
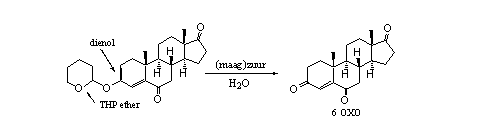
Schema 5
Gewone ethers
Om voor de hand liggende redenen zijn er zijn weinig steroiden als gewone ether op de markt gebracht. Ethers zijn niet erg reactief en er zijn geen enzymen in het lichaam die ethergroepen van een steroid kunnen verwijderen. Anders dan acetalen en enolethers zijn ethers ook stabiel in de zure omgeving van de maag. Oxidatie in de lever zal optreden, maar waarschijnlijk niet zo snel als bij de andere derivaten. Een ether derivaat van een anabool steroid is dus eigenlijk alleen bruikbaar als het derivaat zelf anabole activiteit heeft.
Chemici hebben een redelijk aantal gewone ethers - vooral van testosteron - gesynthetiseerd en getest. Daaruit is gebleken dat 17b-methoxytestosteron (zie Figuur 3) een bescheiden anabole activiteit heeft van ongeveer 25-30% van die van testosteron zelf [4]. De andere testosteron-ethers in Figuur 3 hebben een geringe of geen anabole activiteit. De benzyl-, allyl-, propyl- en 3-hydroxypropyl-ethers (zie Figuur 3 rechtsboven) zijn overigens remmers van 5a-reductase [4].
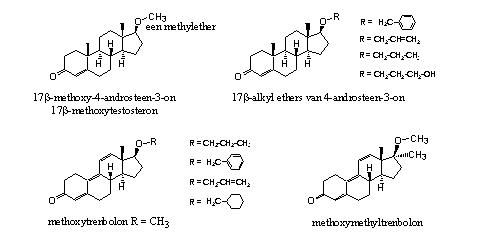
Figuur 3
De methylether van trenbolon (methoxytren) is op de markt gebracht als designersupplement. Na analyse van het product bleek echter dat er geen methoxygroep in de actieve stof aanwezig was; het supplement bevatte gewoon trenbolon [5].
Het farmaceutische bedrijf Roussel-UCLAF heeft in de zestiger jaren van de vorige eeuw meerdere etherderivaten van trenbolon gepatenteerd. In een apart patent is de methoxy-ether van methyltrenbolon (zie Figuur 3 rechtsonder) geclaimd. Deze ether is meer dan twintig keer zo anabool als 17a-methyl-19-nortestosteron [6]. Er is niet aangegeven of de methoxy-ether toxisch is voor de lever, een bijwerking waarvoor 17a-methyltrenbolon zelf berucht is. De ethers linksonder in Figuur 3 zijn oraal actief en hebben anabole en androgene activiteit [7].
Van trenbolon zelf, zijn 13b-ethylderivaat en zijn 7b-methylderivaat zijn een aantal ethers gemaakt die in Figuur 4 zijn weergegeven [8]. Hun aanzienlijke anabole en androgene activiteit is kleiner dan die van 17a-methyltrenbolon, maar de middelen hebben een lange werkingsduur.
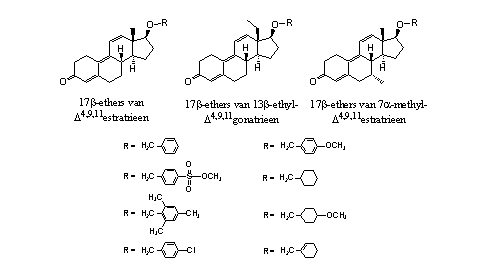
Figuur 4
Silyl-ethers
We willen hier ook de silyl-ethers noemen. Chemici gebruiken ook de silyl-ethergroep veel als beschermende groep voor hydroxylgroepen. Silylethers zijn reactiever dan gewone ethers. Door de aanwezigheid van het silicium atoom (Si) kunnen trimethylsilylethers al in water hydrolyseren tot de vrije hydroxylgroep van bijvoorbeeld een steroid. In het zure milieu van de maag verloopt dat proces nog sneller.
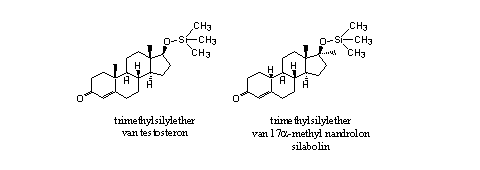
Figuur 5
Geinjecteerde trimethylsilyl-ethers zullen bij de ongeveer neutrale pH in het bloed of in de cel hydrolyseren zonder hulp van enzymen. Meer gehinderde silyl-ethers, met grotere alkylgroepen aan het Si-atoom, hydrolyseren bij neutrale pH zeer langzaam of helemaal niet. Er zijn geen enzymen bekend die silylethers kunnen hydrolyseren.
De trimethylsilyl-ether van testosteron heeft bij injectie een grotere androgene en anabole activiteit dan testosteron zelf [9]. De trimethylsilyl-groep maakt het molecuul apolairder, waardoor het steroidderivaat beter vetoplosbaar is en sneller getransporteerd wordt. Daarna volgt de hydrolyse tot testosteron. Als silylethers niet hydrolyseren hebben ze ook geen anabole activiteit.
Ook de anabole activiteit van de trimethylsilylether van 17a-methyl-nandrolon (silabolin) is onderzocht (zie Figuur 5). Waarschijnlijk zijn de vastgestelde anabole effecten veroorzaakt door het hydrolyseproduct 17a-methyl-nandrolon zelf [10].
Stikstofderivaten
Stikstofderivaten van carbonylgroepen zijn al heel lang bekend. Chemici kunnen deze verbindingen eenvoudig synthetiseren door de reactie van een carbonylverbinding met een reagens dat een aminogroep bevat. De reactie van de carbonylgroep met hydroxylamine (H2N-OH) geeft een oxim, de reactie met hydrazine (H2N-NH2) geeft een hydrazon of een azine. Bij de reactie komt water vrij.
Beide reacties zijn evenwichten. Na een reactie met water (hydrolyse) krijgen we de oorspronkelijke carbonylverbindingen terug (zie Schema’s 6 en 7).
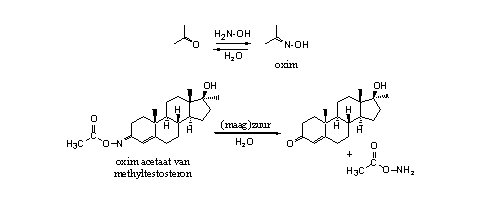
Schema 6
Searle heeft een aantal oximen en oxim-esters gepatenteerd [11] [12]. Volgens de patenten hebben de steroiden anabole, androgene, esterogene, hypocholesteroleme en antibiotische activiteiten, maar waarop de fabrikant die uitspraken baseert vertellen de patenten niet. De derivaten zijn voor zover wij weten nooit op de markt gekomen.
Het oxim-acetaat van methyltestosteron krijg je door eerst een oxim te maken en daarna de hydroxylgroep van het oxim om te zetten in een ester.
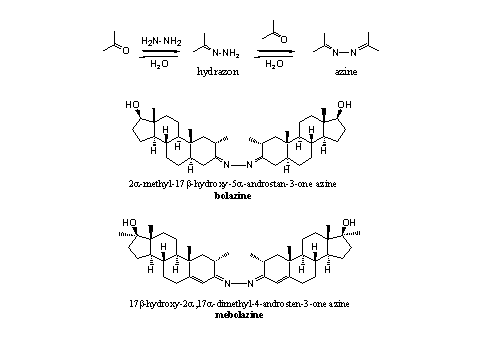
Schema 7
De twee azines in Schema 7 zijn als bolazine en mebolazine op de markt verschenen. Ook deze stikstofderivaten zullen waarschijnlijk al in de maag hydrolyseren. De actieve anabolen zullen daar al vrijkomen.
[1] Kupchan M., Casy A.F. en Swintosky J.V. Journal of Pharmaceutical Sciences (1965) 54 514-524.
[2]T.W. Greene en P.G.M. Wuts, Protective Groups in Organic Synthesis, third edition, John Wiley & sons.
[3] Ercoli A. patent GB 927165 19630529.
[4] Solo A.J., Bejba N. en May M. Journal of Medicinal Chemistry (1975) 18 165-168.
[5] W.Koert en Ae. de Groot. Sport en Fitness (2007) 25 141 68-70; Ergogenics 19/8/2007.
[6] Bucourt R. en Costerousse G. Roussel-UCLAF, Frans patent FR 5320 19670925.
[7] Nedelec L.; Tessier J. en Costerousse G. Roussel-UCLAF, Zuid Afrikaans patent ZA 6701974 19680417.
[8] Costerousse G. en Gase J-C. Roussel-UCLAF, US patent 3629244.
[9] Chang E. en Jain V. K. Journal of Medicinal Chemistry (1965) 9 433-435.
[10] Shishkina A.A., Ivanenko T.I., Zarubina N.A., Volzhina O.N., Angarskaya V.G., en Pivnitskii K.K. Khimiko-farmat Sevticheskii Zhurnal (1986) 20, 232-237.
[11] Mazur R.H. (Searle) US patent 3211756 19651012.
[12] Mazur R.H. (Searle) GB 996256 19650623.
|
|