Het Anabolenboek
Willem Koert
Aede de Groot
Wageningen, 15/9/2007
18. Designersteroïden
Aede de Groot, Willem Koert
Met de Balco-affaire in 2003 heeft de discussie over designersteroïden het grote publiek bereikt. De meeste lezers zullen zich daarbij nauwelijks iets kunnen voorstellen. Journalisten en veel chemici evenmin.
Bij het woord design denken de meeste mensen niet aan chemici die nieuwe verbindingen ontwerpen om speciale taken uit te voeren. Toch is de ontwikkeling van nieuwe moleculen voor medische toepassingen in opkomst. Dat proces is gebaseerd op wetenschappelijk inzicht in de interacties tussen moleculen, zoals bijvoorbeeld tussen anabole steroïden en de androgeenreceptor.
In feite is de jarenlange ontwikkeling van anabole steroïden één groot ontwerpproces geweest. In het begin kwam het ontwerpen neer op het modificeren van bestaande structuren en die testen in een modus van trial and error maar gaandeweg is het bouwen van nieuwe anabole steroïden steeds gerichter geworden. Die ontwikkeling is nu geculmineerd in het bouwen van niet-steroïden met een anabole werking, de Selective Androgen Receptor Modulatoren (SARM’s). Op dit gebied zijn recent interessante ontwikkelingen gepubliceerd. [1]
Zonder dat we het design hebben genoemd, hebben we in dit boek al veel van die steroidontwerpen behandeld in de hoofdstukken 12 en 13. In die hoofdstukken spraken we niet van design, maar van 'chemisch trucs die metabole omzettingen van steroïden verhinderen en de werking van de steroïden verbeteren'. Veel van die anabole steroïden hadden zonder meer de aanduiding 'designersteroid' verdiend.
De huidige aanduiding designersteroid heeft een meer platvloerse oorsprong. De naam is ingevoerd voor anabole steroïden die niet opgespoord kunnen worden in de gangbare dopingtesten, maar wel werken. Atleten kunnen die anabolen dus ongestraft gebruiken en de kluit belazeren. De 'designers' zijn meestal niet zo origineel als ze eigenlijk zouden moeten zijn. Ze vinden hun 'designer'-anabolen' vaak in oude literatuur of in oude patenten van farmaceutische bedrijven. Ze vissen daar een onbekend anabool steroid uit dat nooit op de markt is verschenen. Ze passen het soms iets aan en proberen het maar. Ze maken slim gebruik van bestaande kennis en mogelijkheden.
We zullen in dit hoofdstuk eerst nagaan waarom dopingjagers nieuwe designersteroiden vaak niet zo makkelijk kunnen opsporen. Daarna zullen we uitleggen hoe minder-bonafide producenten nieuwe werkende steroïden kunnen vinden, en we zullen dat met een paar voorbeelden toelichten. Tenslotte zullen we een paar ideeën lanceren voor nieuwe designersteroïden.
Hoe werken de gangbare dopingtests?
De massaspectrometer is het belangrijkste instrument voor het opsporen van anabole steroïden in bloed of urine. Het is het beste instrument voor snelle screening van grote aantallen monsters. De massaspectrometer weegt het molecuul, slaat het stuk en kijkt in welke brokstukken het molecuul uiteenvalt. Als hij de brokstukken op papier weer aan elkaar past, reconstrueert een analytisch chemicus het originele molecuul.
Het eerste wat dopingjagers doen is het wegen van de moleculen in hun monsters. Dat doen ze door te kijken naar de molecuul ion piek, of kortweg de mol piek. De mol piek komt overeen met het molecuulgewicht van het steroid - en dat is weer de optelsom van de gewichten van alle atomen in het molecuul (het atoomgewicht van H=1, C=12 en O=16). Als die optelsom verandert doordat een producent groepen aan het molecuul heeft toegevoegd of weggehaald, dan vind je de mol piek dus op een andere plaats dan waar je die van bekende steroïden verwacht.
De massaspectrometer zoekt bijvoorbeeld standaard naar de aanwezigheid van methyltrenbolon. Dat heeft twee methylgroepen op de plaatsen 13 en 17. Bij het designersteroid norboleton zitten op die plaatsen twee ethylgroepen (zie Figuur 2 verderop). Inmiddels kijken dopingjagers standaard naar norboleton. Maar toen dat nog niet gebeurde, glipten gebruikers van norboleton moeiteloos door de mazen van het dopingnet.
De bruto-formule van methyltrenbolon is C19H24O2, en zijn molecuulgewicht is dus 284. De bruto-formule van norboleton is C21H32O2 en zijn molecuulgewicht is 316. In een monster waarin geen methyltrenbolon zit maar wel norboleton, vind je dus geen mol piek op de plaats van methyltrenbolon bij massa 284. De massaspectrometer kijkt dan niet verder. Daar is hij niet op ingesteld als hij grote aantallen monsters moet screenen. Norboleton met massa 316 wordt dus niet ontdekt.
Er zijn duizenden steroïden bekend. Als je niet weet naar welke je moet zoeken, en dat is met onbekende designersteroïden het geval, dan is het onbegonnen werk al die mogelijkheden na te gaan.
Een nauwkeuriger methode in de massaspectrometrie is het onderzoeken van de brokstukken. Dat is nodig om de structuur van het molecuul ondubbelzinnig vast te stellen. Als er bijvoorbeeld een mol piek verschijnt met massa 284, waar je dus methyltrenbolon zou verwachten, dan kijkt de massaspectrometer verder. Hij kan dan uit het piekenpatroon (de brokstukken) vaststellen of het inderdaad om methyltrenbolon gaat of dat er toevallig een andere stof in het monster zit met eenzelfde mol piek bij 284. Onbekende steroïden geven ook hier onbekende piekpatronen (brokstukken) en worden niet herkend door het apparaat. Zo ontsnapte norboleton lange tijd aan de aandacht. Bovendien stond norboleton niet op de lijst van verboden stoffen.
In principe kunnen dopingjagers alle soorten steroïden in bloed of urine opsporen. Als ze eenmaal een monster van het nieuwe steroid in handen hebben, is het probleem meestal gauw opgelost. Het kost even tijd en moeite, maar met behulp van bioessays, geavanceerde massaspectrometrie en NMR komen ze er wel uit. Dit speurwerk is duur en tijdrovend en niet uit te voeren voor de honderden urine monsters die dopingcontroleurs nemen. Die monsters ondergaan het standaard analyseproces naar bekende verboden middelen die op de lijsten van sportorganisaties staan. Niet minder, maar ook niet meer.
Hoe vind je nieuwe werkende designersteroïden?
Er zijn niet zoveel designersteroïden bekend. Dat is ook logisch. Ze zijn ontworpen om onbekend te blijven. De mogelijkheden om ze te 'ontwerpen' zijn echter tamelijk ruim, zoals we verderop zullen zien. De grootste beperking ligt meestal in de beschikbaarheid van goedkope en goed toegankelijke uitgangstoffen voor hun synthese. Als ondeskundig personeel die synthese uit moet voeren in illegale, vaak primitieve, laboratoria of kleine fabriekjes, dan mag het niet al te lastig zijn. Het designersteroid moet in een paar eenvoudige reactiestappen te maken zijn uit een uitgangssteroid dat al op de markt is.
Designersteroïden moeten ook werken. Het zijn vooral topsporters, of zij die dat willen worden, die deze steroïden gebruiken of zouden willen gebruiken. Die sporters willen resultaat zien - en dat is een probleem. Producenten van designersteroïden kunnen hun middelen niet uitvoerig testen op mensen. Zo’n onderzoeksprogramma zou de hele zaak openbaar maken.
Er zijn echter in de vijftiger en zestiger jaren van de vorige eeuw, de hoogtijdagen van de steroidchemie, verschrikkelijk veel anabole steroïden gemaakt, vooral door farmaceutische bedrijven, maar ook in universitaire laboratoria. Dat onderzoek was bedoeld om medicijnen te ontwikkelen tegen spierzwakte, bloedarmoede, overgangsklachten, hormoon-gerelateerde kankers en geslachtsafwijkingen. Sporters en producenten van voedingssupplementen en designersteroïden hebben echter snel begrepen dat deze steroiden ook voor hen interessant zijn. Veel van dat onderzoek is gepubliceerd in de vorm van patenten en wetenschappelijke artikelen. Verderop zullen we met een aantal voorbeelden duidelijk maken hoe illegale producenten die informatie gebruiken voor het vinden of ontwerpen van nieuwe designersteroïden.
Veel van die gepubliceerde steroïden zijn getest op hun anabole/androgene activiteit, maar vaak alleen in proefdieren, meestal ratten. Het is dan bekend dat ze activiteit hebben maar de bijwerkingen in mensen zijn niet bekend. De rat is wat dat betreft niet zo’n goed proefdier. Testen op mensen zijn duur en die testen zijn, ook in vroeger tijden, slechts voor enkele steroïden uitgevoerd. De bijwerkingen van een steroid in mensen komen pas bij die testen aan het licht en daarover is maar weinig gepubliceerd. Het woord 'bijwerking' komt in patenten van steroïden nauwelijks voor.
De reden dat sommige actieve anabolen niet op de markt zijn gekomen is vaak alleen bekend bij de farmaceutische bedrijven die ze gemaakt en getest hebben. Vaak hadden de middelen gewoon teveel bijwerkingen. De producenten van designersteroïden trekken zich daar niet veel van aan. De gebruikers vinden het kennelijk ook geen bezwaar, of ze steken hun kop in het zand.
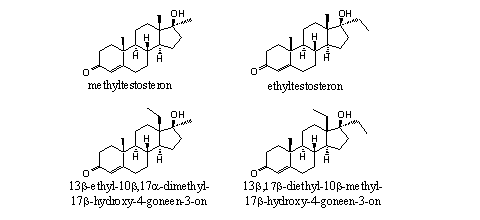
We zullen nu dieper ingaan op de geschiedenis van de drie designersteroïden in Figuur 1 om het bovenstaande toe te lichten. Dopingjagers kunnen deze steroïden tegenwoordig goed opsporen. Ze voldoen dus eigenlijk niet meer aan de definitie van designersteroïden, want ze zijn niet meer onbekend en tegenwordig goed op te sporen. Beschouw ze maar als designersteroïden die van hun voetstuk zijn gevallen.
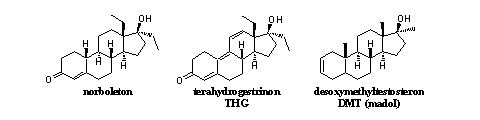
Figuur 1
Norboleton
Norboleton voldeed op één punt niet aan de voorwaarden voor een goed designersteroïd. Het was een bekende verbinding. Het steroid is in de jaren zestig ontwikkeld door het Amerikaanse farmaceutische bedrijf Wyeth [2], die het uit liet testen door de omstreden Leonard LeVann, de medisch directeur van het Canadese zwakzinnigeninstituut Red Deer. [3] LeVann gebruikte de kinderen in zijn instituut als proefkonijn voor de farmaceutische industrie. Dat deed LeVann ook met norboleton, en volgens zijn verslagen was norboleton een mild anabool. Tijdens rechtszaken, die de proefkonijnen van LeVann later hebben aangespannen, is echter gebleken dat de directeur bijwerkingen uit zijn verslagen wegliet en slordig te werk ging. [4]
Ondanks de positieve uitkomsten van LeVanns onderzoek is norboleton niet op de markt gekomen. Wellicht is Wyeth de door LeVann verzwegen bijwerkingen toch op het spoor gekomen, en heeft toen besloten dat norboleton te toxisch was.
In de wetenschappelijke literatuur kun je meerdere studies over de biologische effecten van norboleton vinden. [5-8] Toen de chemicus en supplementen-ontwerper Patrick Arnold, die studies in de jaren negentig van de vorige eeuw vond, werd hij meteen enthousiast. 'Op papier is het een real winner', schrijft Arnold in 1995 in de nieuwsgroep misc.fitness.weights, waarin hij toen actief was. 'Het is erg anabool en weinig androgeen.'
Toen Arnold besloot dat hij norboleton als designersteroïde op de markt wilde brengen, ging hij op zoek naar een manier om het anabool te maken. Een algemene methode voor de synthese van deze steroïden was al lang en breed bekend. Je vindt hem in Hoofdstuk 15, schema 6.
Norboleton kan echter ook in één stap gemaakt worden door reductie van norgestrel, een stof die ontwikkeld was voor anticonceptiepillen en die op de markt is (zie Schema 1). Een probleem is dat de drievoudige binding aan ring D wel gereduceerd moet worden, maar de dubbele binding in ring A niet. Chemici weten dat er een verschil is in gevoeligheid voor reductie tussen die drievoudige binding en de dubbele binding. Bij de juiste keuze van de katalysator kan deze reactie selectief verlopen en wordt alleen de drievoudige binding gereduceerd.
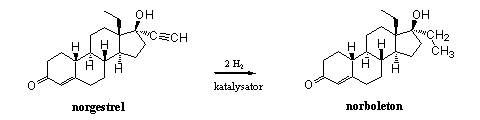
Schema 1
Het designersteroid norboleton werd in gebruikerskringen bekend als 'The Clear'. Geruchten over het hormoon deden al in de jaren negentig de ronde, maar pas in 2002 viel een sporter die norboleton had gebruikt door de mand. [9] Het was wielrenster Tammy Thomas. Toen journalisten spraken met coach Pat McDonough, vertelde die dat het hem was opgevallen dat Thomas de laatste jaren een opvallende lichamelijke transformatie had doorgemaakt. 'Haar bovenlichaam is gegroeid', aldus de coach. 'Ze heeft een zware stem gekregen, en haren op haar gezicht.' Zo weinig androgeen was norboleton dus ook weer niet.
Dat er niet meer sporters op norboleton zijn betrapt, was te danken aan een lek in de organisatie van de dopingjagers. Iemand die werkte op het lab van de dopingjagers waarschuwde de organisatie die norboleton verkocht dat er een test in de pijplijn zat. E-mails waarschuwden trainers en de sporters dat ze de flesjes met Arnolds anabool moesten weggooien. The Clearman, zoals de organisatie Patrick Arnold noemde, werkte echter al aan een nieuw product. Dat was THG. [10]
Tetrahydrogestrinon (THG)
THG was een echt designersteroid. Het was een nieuwe, en tot zijn ontdekking door dopingjagers, onbekende verbinding. Een reeks steroïden die er verrassend veel op lijken staat in een patent van de Franse farmaceut Roussel-UCLAF uit 1969. [11] Dat patent noemt de 13b-ethyl-17a-methyl (zie Figuur 2) en de 17a-ethyl-13b-methyl analogen van THG, maar in het patent staat niets over de 13b,17b-diethyl-verbinding, ofwel THG zelf. Hoewel het patent THG niet noemt, valt de verbinding er wel onder. Het patent vermeldt overigens duidelijk de grote anabole activiteit van de 13b-ethyl-17a-methyl-analoog van THG (zie Figuur 2).
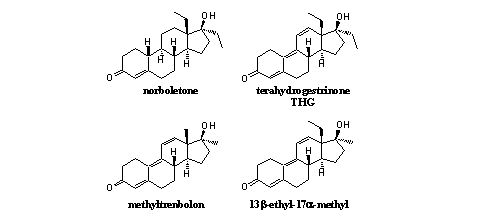
Figuur 2
Uit tests van andere series anabole steroïden, waarin onderzoekers 17a-methyl-analogen hebben vergeleken met 17a-ethyl-analogen, komt naar voren dat de ethylverbindingen vaak minder activiteit hebben dan de overeenkomstige methylverbindingen – maar van een groot verschil is geen sprake.
Een derde aanwijzing voor de mogelijke anabole activiteit van THG was de goede activiteit van norboleton en van (methyl)trenbolon. De chemische structuur van THG is een combinatie van de A-, B- en C- ringen van trenbolon met de D-ring van norboleton (zie Figuur 2). De ontwerpers van THG hebben er op gegokt dat THG ook anabole activiteit zou hebben. Later is gebleken dat dit inderdaad het geval is.
THG is geen eenvoudig steroid. Er is een aanzienlijk aantal reactiestappen voor nodig om het te produceren. Arnold loste dat probleem op. Net zoals hij dat bij norboleton had gedaan, maakte hij THG door selectieve reductie van gestrinon (zie Schema 2). Gestrinon is de actieve stof in sommige gynaecologische preparaten. Meerdere fabrikanten brengen het in aanzienlijke hoeveelheden op de markt.
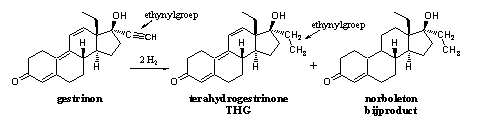
Schema 2
Uitgaande van gestrinon kunnen chemici in één reactiestap tetrahydrogestrinon maken, net zoals ze één stap norboleton kunnen maken: door een katalytische reductie van de drievoudige binding (de ethynylgroep) met twee moleculen waterstof (2 H2). [12-14] Hierdoor komen er vier H-atomen (tetrahydro) aan de ethynylgroep, die daardoor verandert in een ethylgroep. Gestrinon verandert dan in tetrahydrogestrinon of THG (zie Schema 2).
Chemici hebben wel eerst moeten uitzoeken hoe ze die reductie precies moesten uitvoeren, want ook de dubbele bindingen in de B- en C-ring zijn gevoelig voor reductie. De reductie is daarom in het geval van THG lastiger dan in het geval van norboleton. In het preparaat waarin THG voor het eerst is opgespoord, zat ook een beetje norboleton. Dat is het product dat ontstaat bij reductie van de dubbele bindingen in de B- en de C-ring. [12]
In Europa is het gebruik van THG beperkt gebleven tot de atletiek, maar in de VS waaierde het gebruik ook uit naar football en baseball. Volgens gebruikers was het een krachtig middel, misschien zelfs te krachtig voor atleten. 'Ik ging er vocht door vasthouden', zei de sprinter Tim Montgomery bijvoorbeeld tijdens een hoorzitting. 'Mijn spieren voelden aan alsof ze uit elkaar konden klappen. Ik werd er groter en sterker door, maar niet sneller. Het was een middel voor bodybuilders, niet voor sprinters.' [13]
Dopingjagers konden THG niet zien. Ze kenden de stof niet, en met de verbinding was iets merkwaardigs aan de hand. De gangbare dopingtesten konden THG ook niet zien. In die tests maakt het laboratorium eerst een trimethylsilyl-derivaat van het steroid in het monster. Het trimethylsilyl-derivaat van THG is echter niet stabiel bij hogere temperatuur, en ontleedt in de gaschromatograaf tijdens de analyse. [14]
Dopingjagers kregen een kleine hoeveelheid THG te pakken doordat een coach de dopingjagers een restje toespeelde. In het monster was voldoende materiaal aanwezig om de structuur van THG op te helderen. [14] Toen eenmaal bekend was om welke stof het ging was het analyse probleem opgelost. Chemici konden grotere hoeveelheden THG maken en ter beschikking stellen aan dopingjagers voor het ontwikkelen van tests en dat is gebeurd. [15-17]
Er is meteen ook onderzoek gestart naar de anabole activiteit en de mogelijke bijwerkingen van THG. [18-21] Dit is gedaan uit nieuwsgierigheid, om na te gaan of al die verhalen over een superanabool echt waar zijn, maar ook om een reden te hebben de stof te verbieden. Voor dat laatste is het nodig aan te tonen dat de betreffende stof inderdaad anabole activiteit heeft. In al deze onderzoeken is de anabole activiteit van THG ondubbelzinnig vastgesteld, alhoewel de geleerden het niet met elkaar eens zijn over de mate waarin. THG heeft daarnaast androgene eigenschappen en bindt ook met de progesteron-, glucocorticoid- en mineraalcorticoid-receptor. Er zijn aanwijzingen dat THG toxisch is voor de lever. [21]
Samengevat is THG een schoolvoorbeeld van een designersteroid. De stof zelf was onbekend, maar in de literatuur stonden wel gelijkende steroïden met anabole activiteit. Er was daarom een grote kans dat ook THG anabool zou zijn. Bovendien was er een geschikt uitgangsproduct voor de synthese, waardoor de producenten in maar één reactiestap THG konden maken. Daardoor was THG ook een commercieel interessant product.
Desoxymethyltestosteron (DMT, madol)
Toen in de VS het politie-onderzoek naar Balco was begonnen, bleek dat Balco nog een onzichtbaar anabool in voorraad had. Net als norboleton ging het om een steroid dat in de literatuur beschreven is - en voor het eerst in een patent uit 1961. [22]
De wetenschappelijke naam van de verbinding is 17a-methyl-5a-androst-2-een-17b-ol, maar dopingjagers noemen het kortweg 'madol'. Andere namen zijn desoxymethyltestosteron of DMT. Volgens het patent is de anabole activiteit van madol vergelijkbaar met die van methyltestosteron. In een publicatie uit 1961 vinden onderzoekers bij orale toediening van madol aan ratten een androgene activiteit van 0.4 tot 0.6 keer van die van methyltestosteron. De anabole activiteit is twee tot vijf keer die van methyltestosteron. [23]
Madol is chemisch gezien (zie Figuur 1) een andere verbinding dan norboleton en THG. In de structuur van madol zitten geen ethylgroepen op C13 en C17, maar methylgroepen. Vergeleken met gangbare anabolen valt vooral de structuur van ring A op. Daarin zit op C3 geen carbonylgroep. Er is evenmin een D4-dubbele binding in de A-ring te bekennen. Wel zit er in de A-ring een D2-dubbele binding.
Onderzoekers waren verrast door de goede anabole en lage androgene activiteit van madol. Tot dan toe gingen ze ervan uit dat een carbonylgroep op C3 noodzakelijk was voor een goede interactie met de androgeenreceptor en daarmee voor een goede anabole activiteit. De afwezigheid van deze carbonylgroep in madol toonde aan dat dit niet altijd zo hoeft te zijn.
Mede daarom is er in zestiger jaren veel onderzoek gedaan aan madol en aan andere steroïden zonder C3-carbonylgroep. [24-31] Die studies hebben de grote anabole en de geringe androgene activiteit van madol bevestigd. Recent heeft het Centrum voor Preventief Doping Onderzoek van de Duitse Sportuniversiteit in Keulen nogmaals madol onderzocht. [32] De Duitsers stelden in die studie vast dat madol selectief bindt aan de androgeen receptor en geen affiniteit heeft voor de andere steroidreceptoren. Madol heeft een krachtige anabole en geringe androgene activiteit met SARM-achtige eigenschappen, aldus de onderzoekers. [1] Wel bleek dat het steroid de hartspier onevenredig vergrootte – een bijwerking die de onderzoekers niet konden verklaren, maar wellicht reden geeft tot zorg.
De dopingjagers van WADA maakten een test voor het designeranabool en onderzochten oude urinemonsters van topsporters opnieuw. De test sloeg geen enkele keer alarm. Kennelijk heeft Balco madol niet in omloop kunnen brengen. 'This puts us ahead of the dopers', zei Wada-bestuurder Oliver Rabin triomfantelijk in februari 2005 in een interview. [33]
Enkele maanden later, op 18 oktober 2005, publiceerde de Washington Post echter een artikel dat de woorden van Rabin logenstrafte - en de supplementenindustrie deed schudden op zijn grondvesten. [34] In dat artikel vertelde de gerenommeerde dopingjager Don Catlin dat hij in zeven supplementen, die via webwinkels aan sporters worden verkocht, designeranabolen had gevonden. Eén daarvan was madol, het designeranabool dat volgens de WADA nooit in omloop was gebracht. Tienduizenden sporters – vooral bodybuilders - hadden het designeranabool inmiddels gebruikt.
DMT zit in supplementen als 'Phera-Plex' en 'Ergomax LMG'. De makers omschrijven de actieve stof op het etiket als 17a-methyl-etioallocholan-2-een-17b-ol of 17-methyl-D2-etioallocholaan. Dit zijn verouderde namen (zie Hoofdstuk 5) waarmee de makers rookgordijnen probeerden te leggen om autoriteiten te misleiden.
Kopers weten kennelijk wèl wat voor stoffen er in Phera-Plex en Ergomax zitten. Ingetikt op Google resulteren de productnamen in tienduizend hits. Meestal voeren ze naar internetfora, ook naar Nederlandse fora, waar gebruikers vertellen over hun toename in spiermassa en kracht, die meer is dan ze van een voedingsupplement hadden verwacht.
Als journalisten Wada-bestuurder Rabin na het artikel in de Post om commentaar vragen, is Rabin minder opgetogen: 'It's not very difficult for some smart chemist to bypass the law', merkt hij nurks op. [34] Daarmee bedoelt Rabin dat de Amerikaanse rechters, wat anabolen aangaat, uitgaan van een lijst van verboden stimulerende stoffen. [35] Wat op de lijst staat mag niet, wat niet op de lijst staat, mag wel. Een kleine chemische wijziging aan een molecuul op de lijst tovert de stof om in iets wat je in de praktijk in een supplement kunt stoppen.
Nieuwe designeranabolen
Het bedenken van nieuwe designeranabolen is betrekkelijk eenvoudig. Zoals we in Hoofdstuk 15 een paar nieuwe prohormonen hebben bedacht, speculeren we hieronder over nieuwe designersteroïden. Die hebben bijvoorbeeld:
- een extra methylgroep, meestal op C7, C1, C2 en natuurlijk C17, maar mogelijk ook op C4 en C6
- een extra ethylgroep, meestal op C13 en C17
- meerdere extra methyl- of ethylgroepen op combinaties van bovengenoemde plaatsen,
- geen C19-methylgroep
- geen C19-methylgroep, maar ook ergens in het molecuul extra methyl- of ethylgroepen.
Bovenstaande opsomming gaat over het aanbrengen of weglaten van methyl- of ethylgroepen. Andere mogelijkheden zijn:
- het aanbrengen van een of meerdere extra dubbele bindingen,
- het aanbrengen van een extra hydroxyl- of carbonylgroep,
- het invoeren van een extra F- of Cl-atoom.
Dit zijn bekende variaties die chemici allemaal wel eens hebben toegepast, zij het op maar enkele steroïden. Daarnaast zijn er nog tientallen andere substituenten die chemici aan een steroid kunnen hangen, maar daaraan zullen we niet uitgebreid aandacht besteden. De ervaring heeft geleerd dat een flink aantal variaties in het steroid mogelijk is met behoud of verbetering van de anabole activiteit, mits de veranderingen niet al te extreem zijn.
Het is niet handig om variaties in de structuur voor een nieuw designersteroid aan te brengen waardoor enzymen in het lichaam dit steroid kunnen omzetten in een bekend steroid. Dat leidt zonder meer tot een positieve dopingtest. Het designersteroid is dan meer een prohormoon. In Hoofdstuk 15 hebben we die omzettingen behandeld. Daar hebben we al voor het omzetten naar een detecteerbaar hormoon gewaarschuwd.
Het komt er op neer dat ook de enzymatische omzettingsproducten van designersteroïden, de metabolieten, onbekende steroïden moeten zijn.
Analogen van madol
Madol is een geschikt steroid om de mogelijkheden voor het ontwikkelen van nieuwe designeranabolen te illustreren. We beperken ons in eerste instantie tot varianten met een 13b-methyl- of -ethylgroep en/of een 17a-methyl- of -ethylgroep in steroïden met of zonder 19-methylgroep. Er zijn dan acht variaties van madol mogelijk, en die staan in Figuur 3. Een zoektocht in de literatuur wijst uit dat de vier omkaderde 17a-ethyl-analogen onbekend zijn. Misschien hebben farmaceutische bedrijven ze ooit gemaakt, maar ze hebben er – voor zover wij weten - nooit over gepubliceerd.
Naast madol noemt het patent van Huffman [22] ook 17a-alkyl-gesubstitueerde 2-androsteen-17b-ol steroïden, waaronder het 17a-ethyl-steroid. Ook de 19-nor-anabolen van madol [29] [31] en een aantal andere ring A-gemodificeerde analogen [27] zijn ooit gesynthetiseerd.
De 19-nor- en de 2-methyl-analogen van madol hebben net als madol zelf een goede anabole en een geringe androgene activiteit.
Een reden voor de onbekendheid van de 13-ethyl-steroïden is misschien dat onderzoekers hebben verondersteld dat ze te veel bijwerkingen hebben. Een andere reden zou kunnen zijn dat een geschikte uitgangstof voor de synthese van deze steroïden, een basisskelet met een 13b-ethylgroep, niet voorhanden was. Die uitgangsstof is er ondertussen wel.
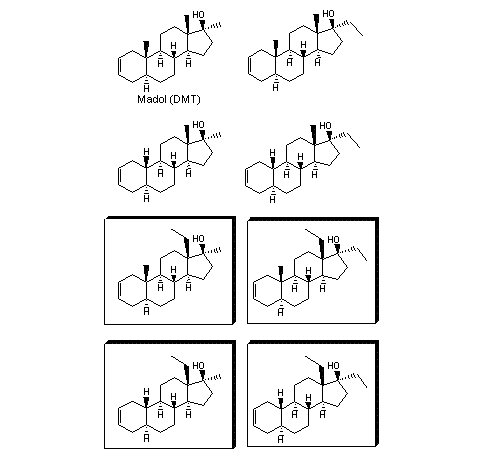
Figuur 3
De vier omkaderde steroiden zijn niet bekend. Alles wat we hier over deze verbindingen zeggen is speculatief.
De omkaderde steroïden zijn niet op te sporen met de gangbare routinematige dopingtests. Het zijn nieuwe, onbekende verbindingen, die de massaspectrometers niet herkennen. Misschien dat een nieuwsgierige massaspectrometrist eens kijkt of er ook mol pieken tevoorschijn komen met massa 14 of 28 hoger, die overeenkomen met een extra methyl- of ethylgroep in een steroid. Ook dan is de kans op ontdekking nog steeds klein, want de analist weet niet aan welk steroid die groepen vastzitten.
Nieuwe designersteroïden moeten werken en zo weinig mogelijk bijwerkingen hebben. Hierover kunnen we niets zeggen, want alleen tests op mensen kunnen uitsluitsel geven. Dierproeven geven indicaties, maar zijn niet honderd procent betrouwbaar.
De synthese op grotere schaal van de nieuwe steroïden moet eenvoudig zijn. De nieuwe steroiden bestellen bij een beter toegerust en in steroïden gespecialiseerd chemisch bedrijf is ook een mogelijkheid. We kunnen speculeren over mogelijke synthese-routes, maar alleen chemische proeven kunnen uitwijzen of die voorgestelde werkwijzen ook werkelijk op grotere schaal uitvoerbaar zijn.
De beste manier om een nieuw designersteroid te synthetiseren is: koop een steroid dat zo dicht mogelijk bij het gewenste eindproduct zit. Voor onze madol-analogen betekent dit dat we het beste steroïden kunnen kopen waarin de gewenste substituenten op C10, C13 en C17 al aanwezig zijn. Het zou nog beter zijn als ook de D4-dubbele binding al gereduceerd is, maar op één na zijn de 5aH-13b-ethyl-steroïden niet bekend - en dus ook niet te koop.
We zullen de D4-dubbele binding dus moeten reduceren. Daarna kunnen we, net zoals dat bij de synthese van madol gebeurt, de D2-dubbele binding in de A-ring aanbrengen. We zullen de zojuist genoemde route bij wijze van voorbeeld uitwerken voor de 19-nor-analogen van madol - de verbindingen met een H-atoom op C10 (zie Schema 3). Er zijn andere syntheseroutes mogelijk [36-39], maar die laten we even buiten beschouwing.
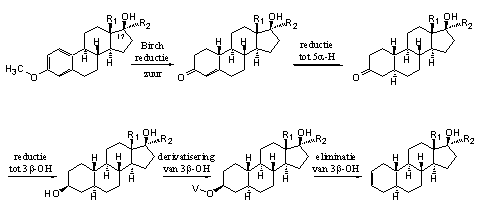
Schema 3
In Hoofdstuk 15 hebben we al uitgelegd hoe je de steroïden middenboven in Schema 3 kunt maken via een Birch-reductie. Hier geven we een algemene structuurformule voor die steroïden. R1 en R2 zijn methyl- of ethylgroepen.
In Figuur 4 hebben we die structuren helemaal uitgeschreven. Daar zie je dat het bekende anabole steroïden zijn. De meeste kun je kopen. De volgende stap is dan de reductie van de D4-dubbele binding, en dus de invoering van het 5a-H-atoom. In de laatste drie stappen moeten we de carbonylgroep op C3 omzetten in een D2-dubbele binding. De klassieke werkwijze daarvoor is: eerst de carbonylgroep reduceren tot een hydroxylgroep, daarna de hydroxylgroep omzetten in een derivaat dat beter uit het molecuul wil vertrekken en tenslotte dat vertrek uitvoeren in een zogenaamde eliminatie-reactie.
Er zitten twee hydroxylgroepen in de verbinding linksonder, maar die op C17 is meer sterisch gehinderd dan die op C3. Het zal daarom waarschijnlijk wel lukken om alleen die C3-groep om te zetten in een beter vertrekkend derivaat. De eliminatie van de gederivatiseerde hydroxylgroep kan twee kanten op, en er zal ongetwijfeld ook een beetje van een steroid met een D3-dubbele binding worden gevormd. Die laatste twee stappen zijn niet lastig.
Het kost dus vier stappen om de steroïden om te zetten in de steroïden met een D2-dubbele binding rechtsonder. Voor een ervaren chemisch bedrijf is dat prima mogelijk, maar voor een clandestien laboratorium of fabriekje is het te moeilijk. Iemand die deze madol-analogen in de handel wil brengen kan beter op zoek gaan naar een chemisch bedrijf dat de stoffen voor hem wil maken.
Synthese van designersteroïden door modificatie van bekende anabolen
Het tussenproduct middenboven in Schema 3 is een algemene structuurformule voor een aantal bekende steroïden. Voor de 19-nor-steroïden hebben we ze uitgeschreven in Figuur 4. Drie hebben een handelsnaam.
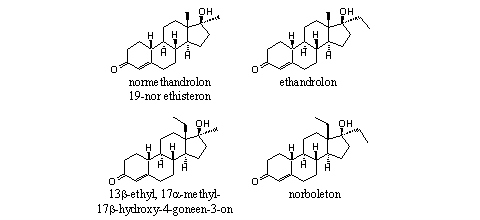
Figuur 4
Voor de testosteron-analogen staan vergelijkbare steroïden in Figuur 5. Ook hier zijn een paar van deze tussenproducten bekende anabole steroiden, maar je moet ze op een andere manier maken dan de 19-nor-steroïden. Alle acht steroïden in de Figuren 4 en 5 zijn bekend.
Figuur 5
De meeste steroïden in de Figuren 4 en 5 zijn zelf actieve anabole steroïden. Het zijn echter ook geschikte tussenproducten voor een aantal andere mogelijk interessante designersteroïden. Die staan in Schema 4. Het is niet moeilijk om in steroïden met een carbonylgroep op C3 een hydroxymethyleen-groep in te voeren op C2. We krijgen dan een hele serie analogen van oxymetholon. De hydroxymethyleen-groep is weer een geschikte hulpgroep om een extra methylgroep in te voeren op C2. Hydroxymethyleen-verbindingen zijn ook gemakkelijk in één stap om te zetten in steroïden met een heterocyclische ring aan ring A. Heterocyclische ringen vind je in stanozolol en danazol.
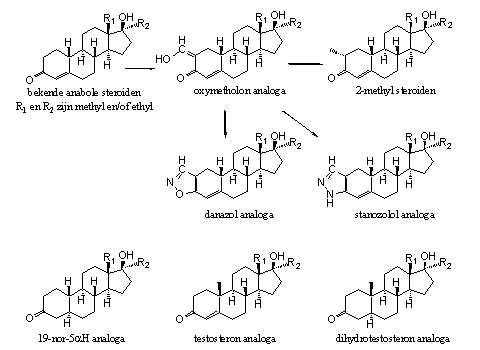
Schema 4
De 19-nor-5a-gereduceerde verbindingen links onderaan Schema 4 kunnen we op dezelfde manier omzetten in nieuwe 5a-gereduceerde designersteroïden. Dezelfde mogelijkheden zijn aanwezig voor de testosteron-analogen midden onderin het schema, en voor de dihydrotestosteron-analogen rechtsonder.
In Schema 4 zie je dat de hydroxymethyleen-steroïden sleutelverbindingen zijn in de synthese van meerdere andere bekende soorten anabole steroïden. We zullen daarom voor die hydroxymethyleen-steroïden nagaan welke bekend zijn en welke niet. We zullen dat doen voor de 19-nor-steroïden, voor de 19-methyl-steroïden, voor de 19-nor-5a-steroïden en voor de 19-methyl-5a-steroïden. Deze zestien mogelijkheden hebben we in Figuur 6 uitgeschreven. De onbekende steroïden staan in een kader. [Klik op de figuur voor een groter afbeelding]
Figuur 6
Het is interessant dat onderzoekers in het verleden uitvoerig hebben gekeken naar de 17a-methyl- en de 17a-ethyl-analogen van alle vier soorten 13-methyl-steroïden (zie kolommen 1 en 2). Het is interessanter dat onderzoekers bijna geen onderzoek hebben gedaan naar de overeenkomstige 13-ethyl-steroïden (zie kolommen 3 en 4). Er zijn twee publicaties bekend waarin het 2-hydroxymethyleen-13b, 17a-diethyl-5aH-gonaan-3-on (tweede rij rechts in Figuur 6) is beschreven. [40] [41] Die artikelen zijn geschreven in het Chinees. Het Engelstalige abstract vertelt weinig over de activiteit van de verbinding.
Ook interessant is tenslotte dat de 2-hydroxymethyleen-analoog van norboleton (2-hydroxymethyleen-13b,17a-diethyl-4-goneen-3-on) (zie Schema 5), niet bekend is in de literatuur. Dit steroid kun je in één stap maken uit norboleton. Is dat gebeurd, dan kun je ook de andere analogen in Schema 4 zonder problemen synthetiseren.
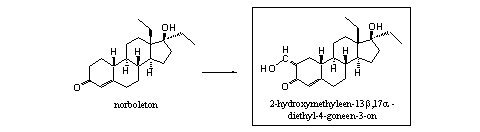
Schema 5
De voorbeelden in Schema 4, Figuur 6 en Schema 5 laten zien hoeveel er mogelijk is op het gebied van designersteroïden. Sinds de Balco-affaire weten we dat er ook personen zijn die van deze mogelijkheden gebruik maken.
Designersteroïden maken met de Pat Arnold-methode
In Schema 6 geven we een laatste voorbeeld van een synthese van een designersteroid. Het is een variatie op de methode die Pat Arnold gebruikte toen hij THG maakte. Wij gebruikten echter niet gestrinon als uitgangsstof, maar een ander hormoon uit de gynaecologie: het steroid tibolon, dat artsen wel eens voorschrijven voor de behandeling van post-menopausale klachten.
De selectieve reductie van de drievoudige binding aan C17 kan op dezelfde manier als voor norboleton of THG. Door de grotere sterische hinder rond de dubbele binding tussen de A- en de B-ring, zal die reductie hier ook wel selectief verlopen. Daarna kunnen we in één of twee stappen de bekende D4,9- en de D4,9,11-dubbele bindingen invoeren. De extra 7a-methylgroep heeft meestal een gunstig effect op de anabole activiteit. Het omkaderde steroid is niet bekend in de literatuur.
Een waarschijnlijke anabole werking, niet omschreven in de literatuur en een breed beschikbare uitgangsstof: aan alle voorwaarden voor een succesvol designer-anabool is voldaan.
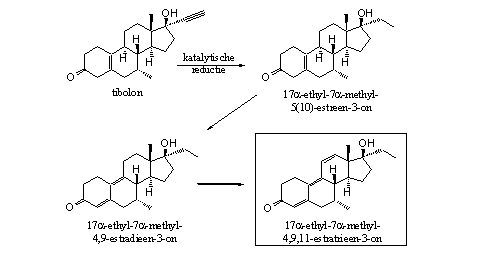
Schema 6
Als je eenmaal weet hoe eenvoudig het is om designer-anabolen te maken, begrijp je waarom dopingjagers – misschien niet de managers, maar wel de techneuten - zich weinig illusies maken. De Balco-affaire, de ontdekking van norboleton en THG, en het betrekkelijke gemak waarmee Pat Arnold zijn onzichtbare anabolen in elkaar schroefde, maakte duidelijk dat de huidige tests weinig gewicht in de schaal leggen.
Sportverslaggever Will Carroll, die een boek schreef over het anabolengebruik in het Amerikaanse baseball, schat dat er minstens drie ondergrondse organisaties in de VS actief zijn die designer-anabolen maken. Die - en vergelijkbare andere - organisaties hebben de bovenstaande mogelijkheden ongetwijfeld al lang geleden grondig bestudeerd. Wat de producenten misschien tegenhoudt zijn de kosten. Voor het aanbrengen van een extra groep in een steroid zijn meestal meerdere reactiestappen nodig. Elke stap verhoogt de kostprijs van het eindproduct en dat maakt geavanceerde designer-anabolen voor de doorsnee-topsporter waarschijnlijk onbetaalbaar.
Aan de andere kant hebben de gebeurtenissen rond THG en norboleton echter laten zien dat je de creativiteit van mensen als Pat Arnold niet moet onderschatten. Toen wetenschappers en farmaceuten al een streep onder de anabole steroïden hadden gezet, zag hij nog mogelijkheden. Met norboleton en THG heeft hij laten zien dat anabolen nog lang niet aan het eind van hun Latijn zijn.
De bovenstaande voorbeelden laten zien dat nieuwe varianten betrekkelijk gemakkelijk te verzinnen zijn. Misschien zijn ze zelfs al in gebruik. Het is echter niet gemakkelijk echt goede anabole steroïden te vinden, met een redelijke verhouding tussen gewenste effecten en ongewenste nevenwerkingen.
De gebruiker is uiteindelijk het proefkonijn. Het zou goed zijn als sportautoriteiten dit gaan beseffen - en zich bezinnen op maatregelen.
[1] Ostrovski J.; Kuhns J.E.; Lupisella J.A.; Manfredi M.C.; Beehler B.C.; Krystek S.R.; Bi Y.; Sun C.; Seethala R.; Golla B.; Sleph P.G.; Fura A.; An Y.; Kish K.F.; Sack J.S.; Mookhtiar K.A.; Grover G.J. en Hamann L.G. Endocrinology (2007) 148, 4-12.
[2] Edgren R.A. (Wyeth Labs.) Acta Endocrinologica (1963) 87, 21.
[3] Int J Clin Pharmacol 1972 Apr;6(1):54-9.
[4] National Post 28/10/1998.
[5] Edgren R.A.; Clancey P.D.; Jones R.C.; Nagra C.L.; Smith H. en Hughes G.A. Recent Progress in Hormone Research (1966) 21, 305-341.
[6] Albanese A.A. Medical Times (1968) 96, 871-881.
[7] Albanese A.A.; Lorenze E.J.; Otto L. A. en Wein E.H. Journal of Medicine (1968) 68, 2392-2406.
[8] Bertolini A.Rivista di Farmacologia e Terapia (1970) 1, 257-262.
[9] Catlin D.H.; Ahrens B.D. en Kucherova Rapid Commun. in Mass Spectrometry (2002) 16, 1273-1275.
[10] Washington Post, 8-3-2003.
[11] Vignau R.; Bucourt R.; Tessier J.;Costerousse G.; Nedelec L.; Gasc J-C.; Joly R.; Warnant J. en Goffinet B. Roussel UCLAF US patent 3,453,267.
[12] Catlin D.H.; Sekera M.H.; Ahrens B.D.; Starcevic B.; Chang Y-C. en Hatton C.K. Rapid Commun. In Mass Spectrometry (2004) 18, 1245-1249.
[13] San Francisco Chronicle, 28-6-2004.
[14] Karpiesiuk W.; Lehner A.F.; Hughes C.G. en Tobin T. Chromatographia (2004) 60, 359-363.
[15] Salvador J-P.; Sanchez-Baeza F. en Marco M-P. Analytical Chemistry (2007) 79, 3734-3740.
[16] Levesque J-F.; Templeton E.; Trimble L.; Berthelette C. en Chauret N. Analytical Chemistry (2005) 77, 3164-3172.
[17] Thevis M.; Bommerich U.; Opfermann G. en Schaenzer W. Journal of Mass Spectrometry (2005) 40, 494-502.
[18] Death A.K.; McGrath K.C.; Kaslauskas R. en Handelsman D.J. Journal of Clin. Endocrinol. Metab. (2004) 89, 2498-2500.
[19] Jasuja R.; Catlin D.H.; Miller A.; Chang Y.-C.; Herbst K.L.; Starcevic B.; Artaza J.N.; Singh R.; Datta G.; Sarkissian A.; Chandsawangbhuwana C.; Baker M. en Bhasin S Endocrinology (2005) 146, 4472-4478.
[20] Labrie F.; Van L-T.; Calvo E.; Martel C.; Cloutier J.; Gauthier S.; Belleau P.; Morissette J.; Levesque M-H. en Labrie C. Journal of Endocrinology (2005) 184, 427-433.
[21] Friedel A.; Geyer H.; Kamber M.; Laudenbach-Leschowsky U.; Schaenzer W.; Thevis M.; Vollmer G.; Zierau O. en Diel P. Toxicology Letters (2006) 164, 16-23.
[22] Huffmann M.N. (1961) US patent 2,996,524.
[23] Edwards J.A. en Bowers A. Chemistry and Industry (1961) 1962-63.
[24] Dorfman R.I. en Kincl F.A. Endocrinology (1963) 72, 259-266.
[25] Kincl F.A. en Pi A.F. (Syntex) Ciencia (1963) 22, 49-53.
[26] Kincl F.A. en Dorfman R.I. (Syntex) Steroids (1964) 3, 109-122.
[27] Cross A.D.; Edwards J.A.; Orr J.C.; Berkoz B.; Cervantes L.; Calzada M. en Bowers A (Syntex) Journal of Medicinal Chemistry (1963) 6, 162-166.
[28] Neumann F. en Wiechert R. (Schering) Arzneimittel Forschung (1965) 15, 1168-1184. [29] Counsell R.E.; Adelstein G.W.; Klimstra P.D. en Smith B. Journal of Medicinal Chemistry (1966) 9, 685-689.
[29] Counsell R.E.; Adelstein G.W.; Klimstra P.D. en Smith B. Journal of Medicinal Chemistry (1966) 9, 685-689.
[30] Nutting E.F.; Klimstra P.D. en Counsell R.E. (Searle) Acta Endocrinologica (1966) 53, 627-634.
[31] Bowers A.; Edwards J.A. en Orr J.C. (Syntex, 1966) United States patent 3 239 542.
[32] Diel P.; Friedel A.; Geyer H.; Kamber M.; Laudenbach-Leschowsky U.; Schaenzer W.; Thevis M.; Vollmer G. en Zierau O. Toxicology Letters (2007) 169, 64-71.
[33] The Guardian, 2-2-2005.
[34] Washington Post, 18-10-2005.
[35] Omschreven in de Anabolic Steroid Control Act of 2004.
[36] Klimstra P.D. en Counsell R.E. (Searle, 1962) United States patent 3 018 298.
[37] Counsell R.E. en Klimstra P.D. (Searle, 1965) United States patent 3 203 966.
[38] Pelc B. en Fajkos J. Czech patent 1967, CS 122950.
[39] Popisec J.; Koblicova Z. en Trojanek J. Czech patent 1968, CS 126388.
[40] Weisheng T.; Xu F. en Liao Q. Yaoxue Xuebao (1984) 19, 35-40.
[41] Li L.; Hou D.; Tao Y. en Liu Z. Zhongguo Yaoke Daxue Xuebao (1987) 18, 66-68.
|
|